









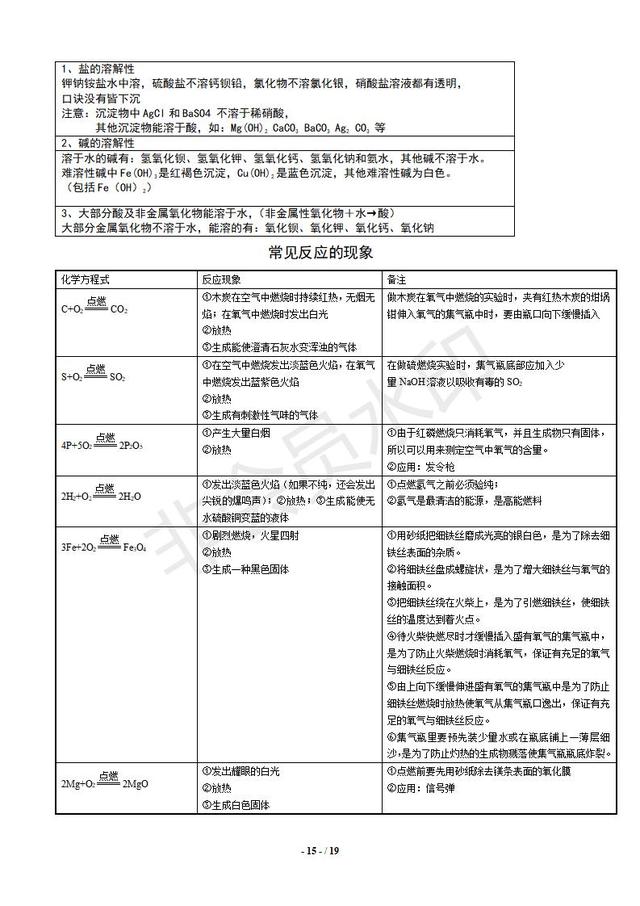
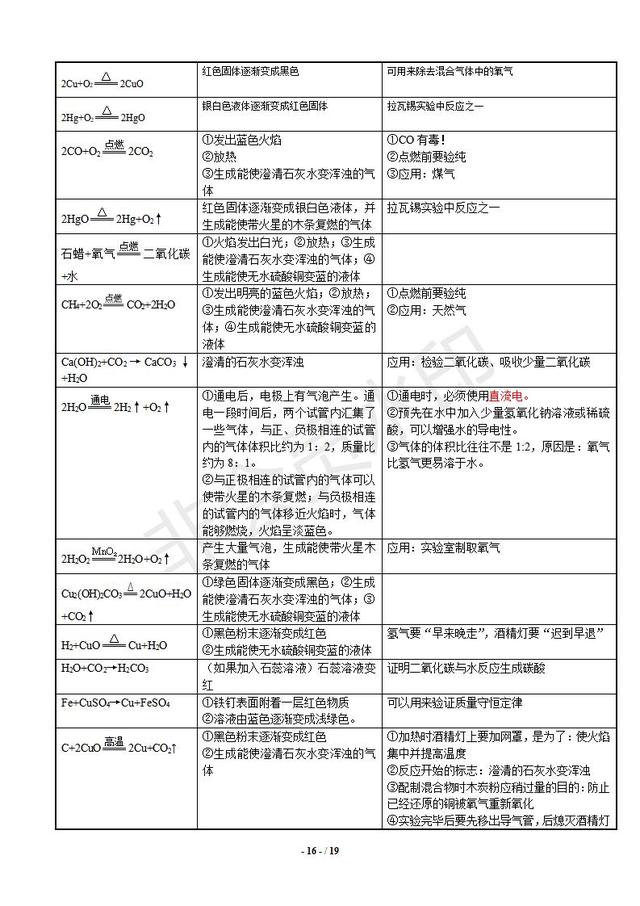
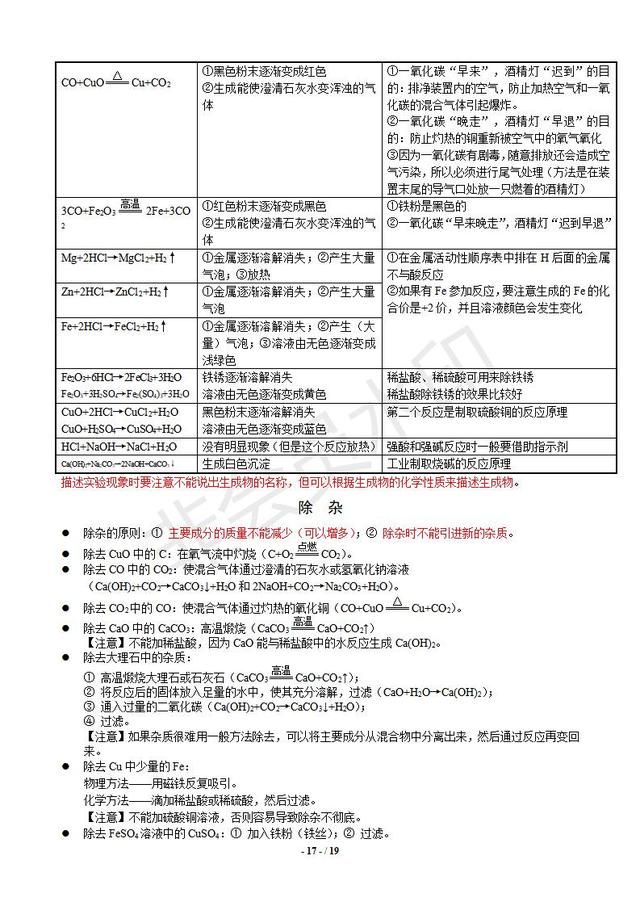

l ④ 可以参考“碱的通性”中的第四条,使溶液中有气体或沉淀生成。
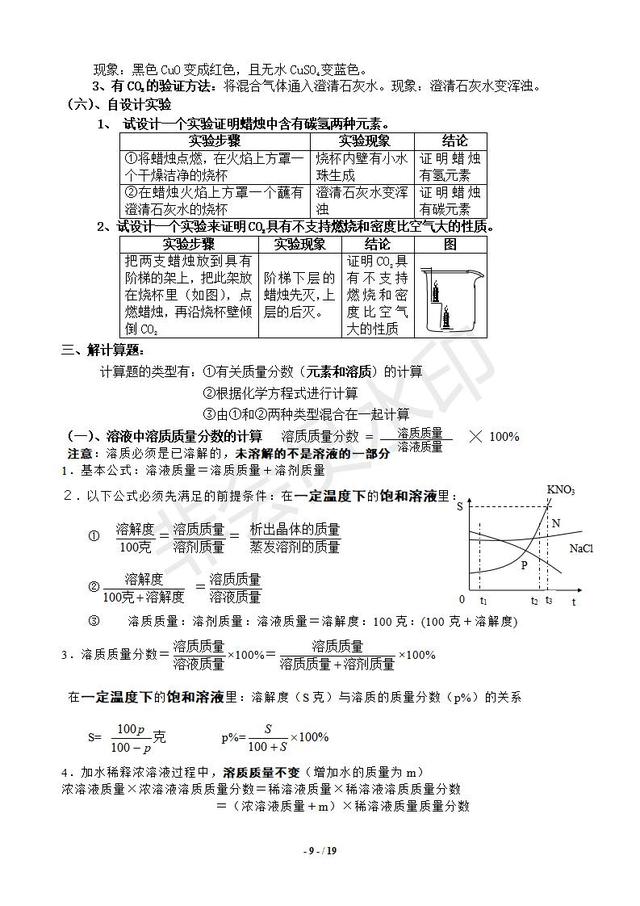
l 鉴定水:通过白色的硫酸铜,如果硫酸铜变蓝,说明有水(CuSO4 + 5H2O → CuSO4·5H2O)
如果要鉴定多种物质,必须把鉴定水放在第一步。如果除水,必须放在最后一步。
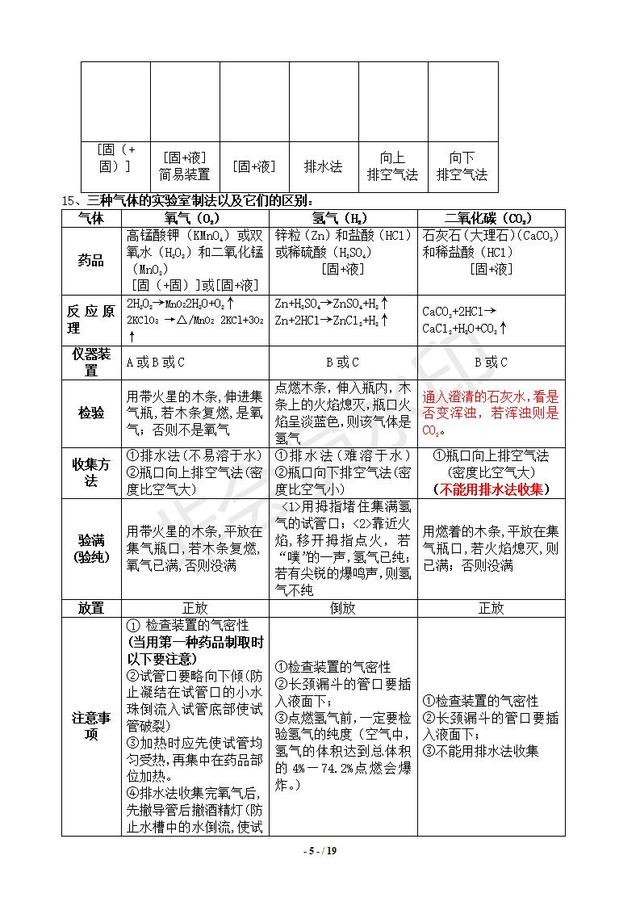
l 鉴定二氧化碳:通入澄清的石灰水中,如果澄清的石灰水变浑浊,说明气体是CO2。
l 鉴定一氧化碳:通过灼热的氧化铜,如果黑色粉末逐渐变成红色,并且产生的气体能使澄清的石灰水变浑浊,说明气体是CO。
区分与鉴定的区别在于,鉴定是要确定一种物质,而区分只需把物质分辨开。区分的要求是无论用什么试剂,采取什么方法,现象必须明显。
应用:离子鉴别、离子共存
一、离子鉴别:要能反应、而且是特征反应。
SO42-:加入BaCl2,产生白色沉淀,再加稀HNO3,沉淀不消失。
Cl-:加入AgNO3,产生白色沉淀,再加稀HNO3,沉淀不消失。
CO32-:加入稀HCl产生无色气体,气体通入澄清石灰水变浑浊。
OH-:加入紫色石蕊变蓝;加入无色酚酞变红。
H+:1)加入紫色石蕊变红;加入无色酚酞不变色。
2)加Zn,生成无色气体。
3)加碳酸钠,生成无色气体。
Ba2+:加入H2SO4,产生白色沉淀,再加稀HNO3,沉淀不消失。
Ag+:加入HCl,产生白色沉淀,再加稀HNO3,沉淀不消失。
NH4+:加入NaOH加热,产生无色能使湿润的红色石蕊试纸变蓝的气体
酸与碱的通性和盐的性质
1、酸的通性(1)酸溶液能使紫色的石蕊试液变红,不能使无色的酚酞试液变色。
(2)酸能与活泼金属反应生成盐和氢气
(3)酸能与碱性氧化物反应生成盐和水
(4)酸能与碱反应生成盐和水(5)酸能与某些盐反应生成新的盐和新的酸
2、碱的通性
(1)碱溶液能使紫色的石蕊试液变蓝,并能使无色的酚酞试液变红色
(2)碱能与酸性氧化物反应生成盐和水
(3)碱能与酸反应生成盐和水
(4)某些碱能与某些盐反应生成新的盐和新的碱
3、盐的性质
(1)某些盐能与较活泼的金属反应生成新的盐和金属
(2)某些盐能与酸反应生成新的盐和新的酸
(3)某些盐能与某些碱反应生成新的盐和新的碱
(4)有些不同的盐之间能反应生成两种新的盐

 加载中,请稍侯......
加载中,请稍侯......
精彩评论