1、盐的概念:由金属阳离子(或NH4+)和酸根阴离子组成的化合物;或者能解离出金属离子(或 NH4+)和酸根离子的化合物。
2、常见的盐:
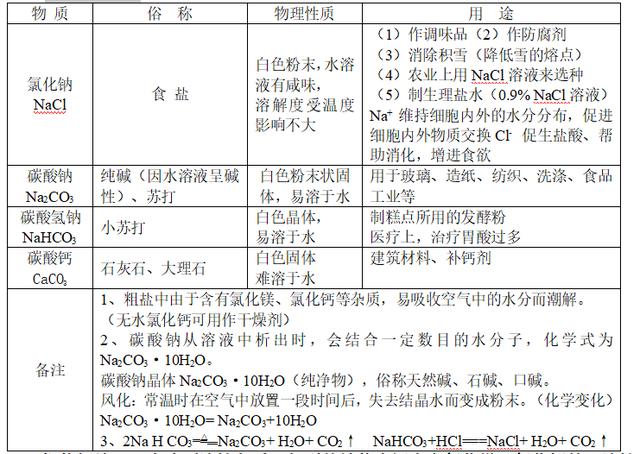
3、粗盐提纯——去除不溶性杂质,得到的精盐中还含有氯化镁、氯化钙等可溶性杂质。
(1)实验步骤:研磨、溶解、过滤、蒸发
(2)实验仪器:
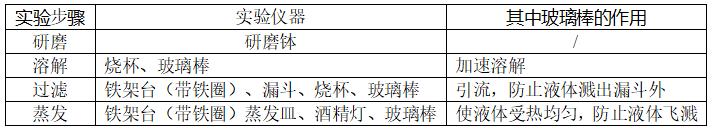

食盐
碳酸钠、碳酸氢钠、碳酸钙的化学性质
1)、碳酸钙的化学性质:
①与酸的反应:2HCl + CaCO3 = CaCl2 + H2O + CO2↑
②高温分解: CaCO3
CaO + CO2 ↑
2)、碳酸钠的化学性质:(这两个反应可用于检验NaOH是否变)
(1)与酸的反应: 2HCl + Na2CO3 = 2NaCl + H2O + CO2↑
(2)与碱溶液的反应;Ca(OH)2 + Na2CO3 = CaCO3↓ + 2NaOH
3)、碳酸氢钠的化学性质:与酸的反应;
HCl + NaHCO3 = NaCl + H2O + CO2↑
4)、检验溶液中存在CO32-的方法:
⑴ 取样少许与试管中,加入稀HCl,若有无色气泡产生,然后将该气体通入澄清石灰水中,石灰水变浑浊,则证明存在CO32-
2HCl + CaCO3 = CaCl2 + H2O + CO2↑ Ca(OH) 2 + CO2 ==== CaCO 3↓+ H2 O
⑵ 加入石灰水或Ba(OH)2溶液,若溶液变浑浊,然后加入稀盐酸浑浊消失,则存在CO32-Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 2HCl +CaCO3 = CaCl2+ H2O+CO2↑
⑶ 加入CaCl2或Ca(NO3)2溶液,若液体变浑浊,则有存在CO32-
CaCl2+ Na2CO3= CaCO3↓+2NaCl Ca(NO3)2+ Na2CO3= CaCO3↓+2Na(NO3)2
4、盐的性质
(1)盐的溶解性
钾钠铵硝全可溶,碳酸钡钙银不溶; 硫酸钡和氯化银,不溶水来不溶酸;
镁铝亚铁和铁铜,五碱均不溶于水; 氢氧化钙硫酸钙,微溶于水要记牢;
(2)盐的化学性质
A、 盐(可溶)+ 金属1 → 金属2 + 新盐(金属1比金属2活泼,K、Ca、Na除外)
反应类型:置换反应
Fe + CuSO4 == Cu + FeSO4 (“古代湿法炼铜”原理)
2Al + 3CuSO4 = Al2(SO4)3 + 3Cu Cu + 2AgNO3 = Cu(NO3)2 + 2Ag
B、 盐 + 酸 → 新盐 + 新酸(满足复分解反应的条件)反应类型:复分解反应
H2SO4 + BaCl2 =BaSO4 ↓+ 2HCl(注BaSO4沉淀:白色,不溶于稀硝酸)
2HCl + Na2CO3 = 2NaCl + CO2↑+ H2O
2HCl + CaCO3 = CO2↑+ CaCl2 + H2O
HCl + NaHCO3 = H2O + NaCl +CO2↑
HCl + AgNO3 = HNO3 + AgCl↓ (注AgCl沉淀:白色,不溶于稀硝酸)
C、 盐 + 碱 → 新盐 + 新碱(反应物需都可溶,且满足复分解反应的条件)
反应类型:复分解反应
2NaOH + CuSO4 = Cu(OH)2↓ + Na2SO4 现象:出现蓝色沉淀
(注:CuSO4 溶液:蓝色 Cu(OH)2沉淀:蓝色)
3NaOH + FeCl3 = Fe(OH)3↓ + 3NaCl 现象:出现红褐色沉淀
(注:FeCl3溶液:黄色 Fe(OH)3沉淀:红褐色)
Ca(OH)2 + Na2CO3 = CaCO3↓ + 2NaOH 现象:澄清石灰水变浑浊
D、 盐 + 盐 → 两种新盐(反应物需都可溶,且满足复分解反应的条件)
反应类型:复分解反应
NaCl + AgNO3 = AgCl ↓+ NaNO3 现象:出现白色沉淀
Na2SO4 + BaCl2 = BaSO4↓+ 2NaCl 现象:出现白色沉淀

5、复分解反应
1、概念:由两种化合物互相交换成分,生成另外两种化合物的反应
2、 特点:首尾相交换,各元素的化合价不变
3、 条件:生成物:有沉淀或有气体或有水生成时,复分解反应才可以发生.
4、反应物:有酸酸必溶,无酸碱盐溶
由于初中常见的酸是可溶性的,因此:
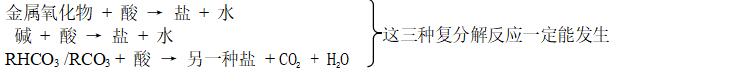
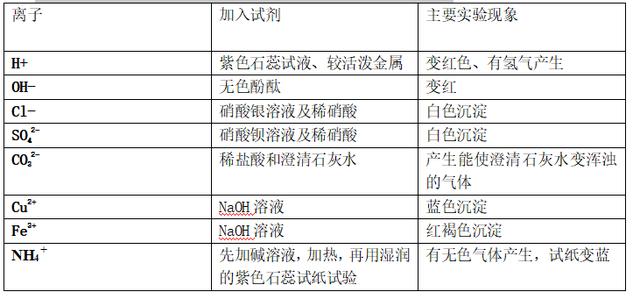
6、常见离子共存与检验
1、 若离子之间发生离子反应,离子间便不能在溶液共存:
(1)生成沉淀物:Cl-与Ag+、 Ba2+ 与SO42-、OH-与Cu2+、Fe3+
(2)生成气体:OH-与NH4+ 、H+和CO32-
(3生成水
2、此外要注意:题目要求的在酸性溶液还是碱性溶液、或者溶液是无色还是有色
常见的有色离子:Fe3+黄色、Fe2+浅绿色、Cu2+蓝色、MnO4-紫色
7、除杂
遵循的原则:不增、不减、简便、易分
1、 物理方法:利用物质的溶解性、磁性、沸点等物理性质的差异分离
Eg:铁粉和碳粉 BaSO4和NaOH粉末
2 化学方法:①化气法:像混合物中加入某种试剂,使混合物中的杂质变为气体逸出
Eg:NaCl中混有少量Na2CO3杂质
方法:加入HCl Na2CO3 +HCl=NaCl+H2O+CO2↑
3 沉淀法:向混合物中加入某种试剂,使该试剂与杂质放映转化成沉淀,再经过虑除掉沉淀,以除杂质
Eg:NaCl中混有少量NaSO4杂质
方法:加入BaCl,过滤除去杂质 NaSO4=BaSO4+NaCl
4、加热高温法:热高温混合物是杂质变为气体除去
Eg:CaO中混有CaCO3杂质
方法:高温加热 CaCO3
CaO + CO2 ↑
5、溶解法:向混合物中加入某种试剂,使杂质与试剂反应而被溶解掉,以除去杂质
Eg:Cu中混有少量CuO杂质
方法:加入稀HCl,再经过过滤而除去 CuO+HCl=CuCl2+ H2O
6. 置换法:向混合物中加入一种单质,是单质与杂质反应,而被除去
Eg:FeSO4中混有少量CuSO4杂质
方法:向其加入足量的铁粉 Fe+ CuSO4=Cu+FeSO4
7、吸收法:将气体混合物通过洗气装置,杂质被洗气装置的试剂吸收而除去
Eg:CO中混有少量CO2
方法:将混合气体通过盛有足量的NaOH溶液的洗气置 2NaOH+CO2=Na2CO3+H3O

8、化肥
一、农家肥料:营养元素含量少,肥效慢而持久、价廉、能改良土壤结构
二、化学肥料:(氮肥、钾肥、磷肥)
1、氮肥 (1)、作用:促进植物茎、叶生长茂盛、叶色浓绿(促叶)。
(2)、缺氮:叶黄
(3)、常用氮肥:
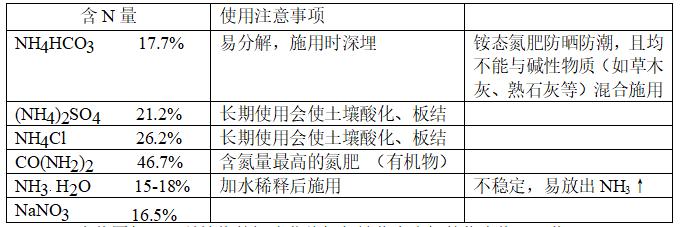
(4)、生物固氮:豆科植物的根瘤菌将氮气转化为含氮的化合物而吸收
2、钾肥 :(1)作用:促使作物生长健壮、茎杆粗硬,抗倒伏(壮秆)。
(2)缺钾:叶尖发黄

5、氮、磷、钾三种化肥的区别方法
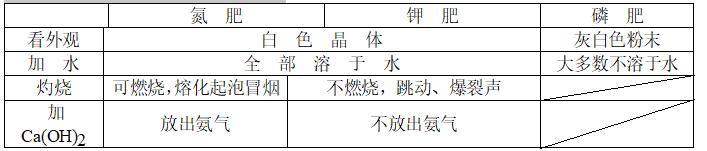
6、 化肥与环境
(1)土壤污染:重金属元素、有毒有机物、放射性物质
(2)大气污染:NO2、NH3、H2S、 SO2
(3)引起水体污染 :N、P过多,导致水体富营养化,赤潮、水华等现象

 加载中,请稍侯......
加载中,请稍侯......
精彩评论